呼吸道合胞病毒(RSV)
呼吸道合胞病毒(Respiratory Syncytial Virus, RSV)是一种非节段性的单股负链RNA病毒,属于副粘病毒科(Paramyxoviridae),肺炎病毒属,因其能将感染的细胞融合而得名。RSV可在全球范围内引起婴幼儿、老年人和免疫功能低下者呼吸道感染,是5岁以下儿童下呼吸道感染的主要致病原因,每年导致约3300万例下呼吸道感染病例,其中中国约占十分之一,即350万例。据估计,我国每年因RSV感染住院的婴幼儿人数在30万到50万之间。
1. RSV病毒的结构
RSV的病毒颗粒形态多样,包括球形、不对称形和丝状形,直径约为130纳米,长度可以从几百纳米到超过10微米不等。
RSV的结构组成主要包括病毒包膜和内部的核糖核蛋白复合体(RNP)。病毒包膜由融合蛋白(F)、附着蛋白(G)和小疏水蛋白(SH)等糖蛋白组成。这些糖蛋白在病毒的吸附、融合和感染过程中起着重要作用。其中,G蛋白是病毒的主要附着蛋白,负责与宿主细胞受体结合;F蛋白则介导病毒囊膜与宿主膜的融合。RSV的核糖核蛋白复合体由RNA和核衣壳蛋白(N蛋白)组成,这些复合体在病毒颗粒内部形成螺旋状结构,保护并复制病毒的RNA [1]。
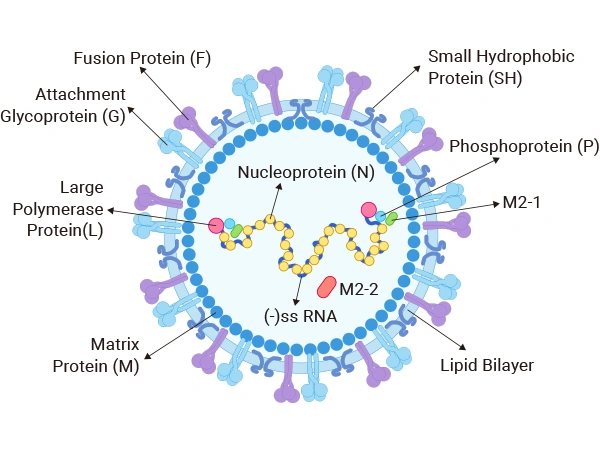
图1. 呼吸道合胞病毒结构
RSV病毒的基因组由具有10个开放阅读框(ORF)的单链负义RNA组成,总长度约为15.2kb。它编码11种结构和非结构蛋白,这些蛋白在病毒的复制、装配和感染过程中发挥着各自的作用。具体列举如下:
| 蛋白名称 | 功能描述 |
|---|---|
| 融合蛋白(F) | 介导病毒与宿主细胞膜的融合,使病毒进入细胞内。是产生中和抗体的重要抗原位点,也是诱导机体产生免疫原性和抗病毒的主要靶点。 |
| 黏附蛋白(G) | 负责将病毒吸附到宿主细胞表面,启动感染过程。G蛋白高度变异,与抗原表位决定簇和病毒基因多样性的关系密切,在区分RSV A、B亚型方面起重要作用。 |
| 小疏水蛋白(SH) | 一种跨膜蛋白,具体功能可能涉及病毒的感染和复制过程,但相对于F和G蛋白,其重要性较低。 |
| 核蛋白(N) | 与病毒的RNA结合,形成核衣壳,保护病毒的遗传物质。 |
| 磷酸蛋白(P) | 与N蛋白和L蛋白一起构成病毒的复制复合物,参与病毒的复制过程。 |
| RNA聚合酶蛋白(L) | 具有RNA聚合酶活性,负责病毒的RNA合成和复制。 |
| 基质蛋白M1(M) | 位于脂质包膜下方,与复制复合物结合,参与病毒的装配过程。 |
| 基质蛋白M2(M2-1) | 与M蛋白一起参与病毒的装配和出芽过程,同时可能具有调节病毒RNA合成的作用。 |
| 基质蛋白M2-2(M2-2) | 参与病毒的复制和转录过程,可能通过调节病毒RNA的合成来影响病毒的复制效率。 |
| 非结构蛋白NS1 | 具体功能尚不完全清楚,但可能参与调节病毒的复制和感染过程。 |
| 非结构蛋白NS2 | 同样具有调节病毒复制和感染过程的功能,但具体机制尚待研究。 |
2. RSV病毒的感染机制
RSV的感染机制涉及多个步骤,如病毒的附着、进入、复制、组装和释放:
向内是由8片单链RNA组成的病毒基因组(仅甲型和乙型)。RNA被核蛋白和异三聚体RNA依赖的RNA聚合酶(三个亚单位:PB1、PB2和PA)包裹,组装成螺旋状的核糖核蛋白(RNP)复合物。核外蛋白(NEP)也存在于病毒内部。
- 病毒附着:通过飞沫传播,首先附着在宿主的上呼吸道上皮细胞表面。病毒表面的G蛋白(糖蛋白)识别并结合到宿主细胞表面的特定受体。这些受体包括硫酸肝素蛋白多糖(HSPGs)和其他可能的受体分子。
- 病毒进入:附着完成后,病毒表面的F蛋白(融合蛋白)发生构象变化,介导病毒囊膜与宿主细胞膜的融合后,病毒的核衣壳进入宿主细胞。除了膜融合,RSV还可以通过内吞作用进入细胞。病毒被宿主细胞的胞吞作用摄入,形成内吞体。在内吞体内,酸性环境促使F蛋白进一步激活,最终导致病毒囊膜与内吞体膜融合,释放病毒核衣壳到细胞质中。
- 病毒复制:病毒核衣壳进入宿主细胞后,RSV的核衣壳解体,释放出单股负链RNA基因组。病毒RNA基因组被病毒RNA依赖的RNA聚合酶(由L蛋白和P蛋白组成)识别并转录成正链mRNA。这些mRNA随后被翻译成病毒蛋白,包括结构蛋白和非结构蛋白。病毒RNA聚合酶还负责合成新的负链RNA基因组,这些基因组将被包装进新的病毒颗粒中。
- 病毒组装与释放:新合成的病毒RNA与N蛋白结合,形成新的核衣壳。新的核衣壳移动到宿主细胞的细胞膜附近,与M蛋白相互作用,招募囊膜上的G蛋白和F蛋白,形成新的病毒颗粒。成熟的病毒颗粒通过宿主细胞膜的出芽过程被释放到细胞外环境中。这个过程中,病毒颗粒获得了宿主细胞膜的一部分作为自己的囊膜。
- 免疫反应与病理:感染触发宿主的先天免疫和适应性免疫反应。先天免疫反应包括产生干扰素和其他炎症介质,而适应性免疫反应则涉及产生特异性抗体和T细胞应答。RSV感染导致气道上皮细胞损伤,炎症细胞浸润,气道分泌物增多,气道狭窄和高反应性。这些病理变化可以引起咳嗽、喘息、呼吸困难等症状,严重时可能导致支气管炎和肺炎。
了解RSV病毒的感染机制对于开发有效的预防和治疗策略至关重要。目前,针对RSV感染的疫苗和抗病毒药物的研发正在取得进展,旨在通过干预这些关键步骤来减轻RSV的传播和致病性。
3. RSV抗病毒药物研究主要靶点及相关药物研究进展
RSV抗病毒药物研究的相关靶点主要包括F蛋白、RNA聚合酶、核苷类似物、宿主因子以及脱氧鸟嘌呤核苷酸合成途径等。这些靶点的研究为开发新型抗RSV药物提供了重要的基础。
- 融合蛋白(F蛋白):蛋白是RSV进入宿主细胞的关键因素,通过介导病毒包膜与宿主细胞膜的融合来完成病毒的进入过程。因此,针对F蛋白的抑制剂是研究的重点之一。例如,GS-5806和BMS-433771都是通过抑制F蛋白介导的膜融合来阻止病毒进入宿主细胞 [2]。此外,RV521也是一种针对RSV-F蛋白的小分子抑制剂,已在临床试验中显示出减少病毒载量和改善疾病严重程度的效果 [3]。
- 核苷酸依赖性RNA聚合酶(RdRp):RSV的RNA聚合酶是另一个重要的药物靶点。通过抑制病毒的RNA复制过程,可以有效阻断病毒的生命周期。例如,结构基础设计策略发现了针对RSV RdRp的新异构体结合位点,开发出了一些具有抗病毒活性的小分子抑制剂 [4]。
- 宿主因子:近年来,越来越多的研究开始关注针对宿主因子的抗病毒药物开发。例如,核糖核蛋白(N蛋白)和G蛋白也是重要的靶点,因为它们在病毒感染过程中起着关键作用 [5]。此外,核仁蛋白(nucleolin)也被发现是RSV的重要受体,针对其RNA结合域的药物可以有效抑制RSV感染 [6]。
- 脱氧鸟嘌呤核苷酸合成途径:一些研究表明,通过抑制宿主细胞中的脱氧鸟嘌呤核苷酸合成途径,也可以有效抑制RSV的复制。例如,probenecid这种FDA批准的药物通过抑制有机阴离子转运蛋白(OATs),显示出对RSV复制的抑制作用 [7]。
4. RSV研究相关重组蛋白
| Target | Product Name | Source | Tag Info | Product Code |
|---|---|---|---|---|
| N | Recombinant Bovine respiratory syncytial virus Nucleoprotein (N) | E.coli | N-terminal 6xHis-SUMO-tagged | CSB-EP339612BKT |
| F | Recombinant Human respiratory syncytial virus A Fusion glycoprotein F0 (F), partial | E.coli | N-terminal 6xHis-B2M-tagged | CSB-EP356041HPO |
| F | Recombinant Human respiratory syncytial virus A Fusion glycoprotein F0 (F), partial | E.coli | N-terminal 6xHis-tagged | CSB-EP356041HPOa0 |
| F | Recombinant Human respiRatory syncytial virus A Fusion glycoprotein F0 (F), partial | Yeast | N-terminal 6xHis-tagged | CSB-YP356041HPO |
| G | Recombinant Human respiratory syncytial virus A Major surface glycoprotein G (G), partial | Baculovirus | N-terminal 10xHis-tagged and C-terminal Myc-tagged | CSB-BP365937HPO |
| G | Recombinant Human respiratory syncytial virus A Major surface glycoprotein G (G), partial | E.coli | N-terminal 6xHis-SUMO-tagged | CSB-EP365937HPO |
| G | Recombinant Human respiratory syncytial virus A Major surface glycoprotein G (G), partial, Biotinylated | E.coli | N-terminal 6xHis-SUMO3-Avi-tagged | CSB-EP365937HPOm4-B |
| F | Recombinant Human respiratory syncytial virus A Fusion glycoprotein F0 (F), partial | E.coli | N-terminal 10xHis-tagged and C-terminal Myc-tagged | CSB-EP319265HPWb1 |
| G | Recombinant Human respiratory syncytial virus B Major surface glycoprotein G (G), partial | E.coli | N-terminal 6xHis-tagged | CSB-EP323293HPX |
| N | Recombinant Human respiratory syncytial virus B Nucleoprotein (N) | E.coli | N-terminal 10xHis-tagged and C-terminal Myc-tagged | CSB-EP340633HPX |
| F | Recombinant Human respiRatory syncytial virus B Fusion glycoprotein F0 (F), partial | Yeast | N-terminal 6xHis-tagged | CSB-YP516611HXK |
| M2-1 | Recombinant Human respiratory syncytial virus B Matrix M2-1 (M2-1) | E.coli | N-terminal 6xHis-tagged and C-terminal 6xHis-tagged | CSB-EP518618HXK |
参考文献:
[1] Crystal structure of a nucleocapsid-like nucleoprotein-RNA complex of respiratory syncytial virus. Science, 2009.
[2] Oral GS-5806 Activity in a Respiratory Syncytial Virus Challenge Study. The New England Journal of Medicine, 2014.
[3] A Randomized, Placebo-Controlled, Respiratory Syncytial Virus Human Challenge Study of the Antiviral Efficacy, Safety, and Pharmacokinetics of RV521, an Inhibitor of the RSV-F Protein. Antimicrobial Agents and Chemotherapy, 2020.
[4] Structure-Based Discovery of Allosteric Inhibitors Targeting a New Druggable Site in the Respiratory Syncytial Virus Polymerase. ACS Omega, 2024.
[5] Progress in studies on drugs and their target points against respiratory syncytial virus. Chinese Journal of Clinical Hepatology, 2020.
[6] Identification of RSV Fusion Protein Interaction Domains on the Virus Receptor, Nucleolin. Viruses, 2021.
[7] Probenecid Inhibits Respiratory Syncytial Virus (RSV) Replication. Viruses, 2022.






